PD-1/PD-L1抑制剂竞争加剧;华海药业HB0025双特异性抗体展现潜力。
CSCO指南作为肿瘤临床实践的重要参考,已成为评估创新药物价值的关键标准。它综合证据强度、药物可及性与专家共识,形成明确的推荐级别,直接影响治疗方案的选择与优先顺序。在当前循证医学框架下,指南不仅是医生的工具书,更是衡量新药临床定位与市场前景的标尺。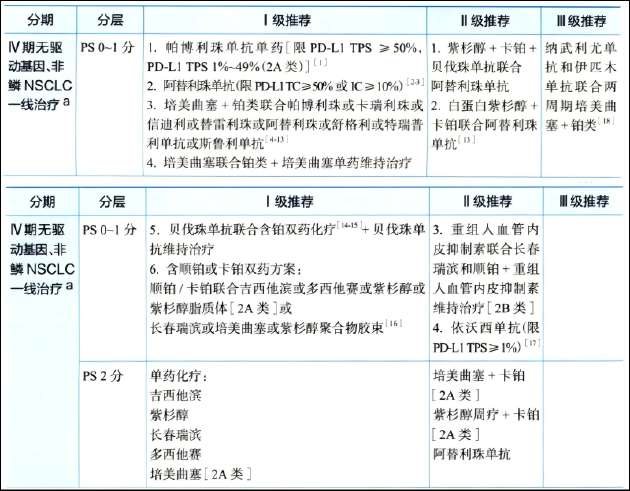
非小细胞肺癌分为鳞状与非鳞状两大亚型,二者在病理起源、特征及人群分布上存在差异。一线治疗策略已超越单纯形态学分类,转向基于分子病理的精准路径。首先通过基因检测排除驱动基因突变,如EGFR、ALK等,若阳性则优先靶向药物;若阴性,再依据PD-L1表达水平决定免疫治疗方案。高表达者倾向单药免疫,低表达或阴性者多采用免疫联合化疗。这种分层已成为主流,无论亚型均适用,但化疗药物组合有所调整。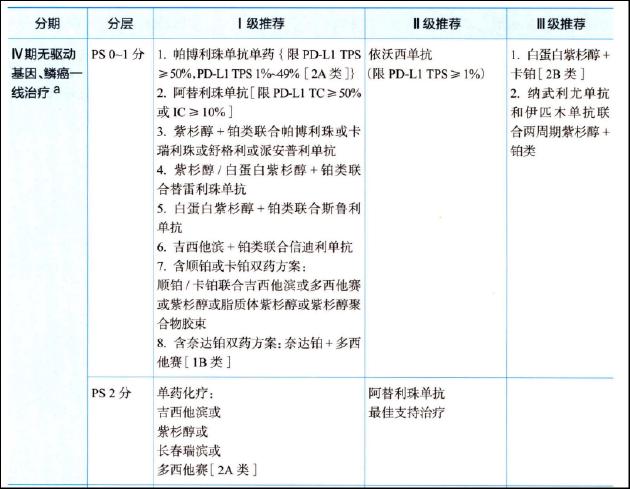

华海药业子公司华奥泰研发的HB0025是一种创新型PD-L1/VEGF双特异性融合蛋白。该药在2025年ESMO会议公布的II期临床数据中,联合化疗一线治疗晚期鳞状NSCLC显示客观缓解率达较高水平,PD-L1高表达亚组表现尤为突出;非鳞状队列也呈现积极信号,疾病控制率保持稳定。安全性数据显示,严重免疫相关不良事件发生率较低,整体耐受性良好。这些初步结果在非头对头比较中,与现有部分PD-1/PD-L1抑制剂联合化疗方案相比,短期疗效指标表现出一定优势。
然而,肿瘤治疗的核心在于长期生存获益。多项研究表明,客观缓解率与无进展生存期的改善,并不总是与总生存期显著相关。HB0025虽在II期研究中展现出鼓舞人心的短期数据,但需等待III期研究确认长期生存优势,方能确立其真正临床价值。在当前环境下,药物需通过更严格的证据积累,才能在指南中获得更高推荐级别。

PD-1/PD-L1抑制剂领域已形成激烈竞争格局。多家药物获批并纳入CSCO指南推荐,用于驱动基因阴性NSCLC一线治疗,包括多种国产与进口选项,大部分已进入医保目录,构建起坚实的市场基础。同时,生物类似药加速推进,进一步加剧价格竞争。HB0025凭借双靶点机制,可能实现免疫与抗血管生成的协同效应,但要在拥挤赛道中脱颖而出,仍面临诸多挑战,包括现有方案的先发优势与医保准入壁垒。
同类双特异性抗体中,部分产品已获批,但主要定位于特定亚群或后线治疗。对于无驱动基因NSCLC,HB0025若能提供更优的综合获益,或在指南更新中占据有利位置。非小细胞肺癌是中国发病率最高的恶性肿瘤,每年新发病例众多,中晚期占比高,驱动基因阴性患者适合免疫联合方案,市场空间广阔。若HB0025未来实现一定份额渗透,年销售额潜力可观,成为公司重要增长点。
总体而言,HB0025的出现为肺癌治疗注入新活力。尽管竞争环境严峻,但其独特机制与初步数据为其带来差异化机会。后续III期研究结果将成为决定性因素,影响其临床应用广度与市场表现。肿瘤领域创新永无止境,持续关注此类双靶点药物进展,有助于把握精准医疗趋势。
